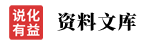
下游产品 | 磷酸钙-->洗衣粉-->有机硅柔软剂 RS-->橡胶浆 202BA-->阴离子有机硅柔软剂306羟乳-->餐具洗洁精-->粘合剂 BA-->分散松香胶-->乳化剂TX-7-->洗净剂 826-->高效煮练剂 FB-->高温匀染剂FZ-802-->橡胶浆 109BA-->柔软剂 FS-->工业洗毛粉-->净洗剂 YR-301-->纸用透明剂-->马来酸酐/苯乙烯磺酸共聚物-->荧光增白剂 SRBN, BCF, CA, DW, DK, OD, 4A, 4,4'-双-(4,6-二苯胺基-1,3,5-三嗪-2-氨基)-二苯乙烯2,2'-二磺酸钠-->十八烷基甲苯磺酸钠-->抗蚜威可湿性粉剂 |
十二烷基苯磺酸钠工业制备
在工业生产上,直链烷基苯磺酸盐也不是单一的产物,而是直链烷烃与苯在链中任意点上相连,其结果产生了不同仲烷基比例的混合物。商品烷基苯通常是C10~C13烷基的混合烷基苯。
在工业生产上,直链烷基苯磺酸盐也不是单一的产物,而是直链烷烃与苯在链中任意点上相连,其结果产生了不同仲烷基比例的混合物。
十二烷基苯磺酸钠制备流程图

实验操作
一、实验目的
1、 掌握烷基苯磺酸钠(LAS)的制备方法。
2、 了解用不同磺化剂进行磺化反应的机理和反应特点。
3、 了解十二烷基苯磺酸钠性质、用途和使用方法。
二、实验原理
磺化反应是向有机分子中的碳原子上引入磺酸基(-SO3H)的反应。生成的产物是磺酸(R-SO3H)、磺酸盐(R-SO3M;M表示NH4或金属离子)或磺酰氯(R-SO2Cl)。
磺化是亲电取代反应。 SO3分子中硫原子的电负性比氧原子的电负性小,所以硫原子带有部分正电荷而成为亲电试剂。
常用的磺化剂是浓硫酸、发烟硫酸、三氧化硫、氯磺酸。
磺化的主要方法有:
1 .过量硫酸磺化法(磺化剂是浓硫酸和发烟硫酸);
2 .共沸脱水磺化法;
3 .三氧化硫磺化法;
4 .氯磺酸磺化法;
5 .芳伯胺的烘焙磺化法。
磺化反应的主要目的有:1.使产品具有水溶性、酸性、表面活性或对纤维素具有亲和力。 2.将磺基转化为-OH、-NH2、-CN或-CL等取代基。3.先在芳环上引入磺基,完成特定反应后,再将磺基水解掉。
磺化反应的主要影响因素有:
硫酸的浓度和用量对磺化反应的速度有很大影响
随着磺化反应的进行,生成的水逐渐增加,硫酸的浓度逐渐下降,使磺化开始阶段和磺化末期,磺化反应速度就可能下降几十倍,甚至几百倍而几乎停止反应。这时的硫酸被称为“废酸”,用“ π值”表示。为了消除磺化反应生成的水的稀释作用的影响,必须使用过量很多的硫酸(х值)。
π值是将废酸中所含硫酸的质量换算成SO3的质量后的质量百分数
磺化反应温度和时间的影响
磺化温度会影响磺基进入芳环的位置和磺酸异构体的生成比例。特别是在多磺化时,为了使每一个磺基都尽可能地进入所希望的位置,对于每一个磺化阶段都需要选择合适的磺化温度。低温、短时间的反应有利于α取代,高温、长时间的反应有利于β取代。
磺化产物的分离: 稀释析出法(有些磺化产物在稀硫酸中的溶解度很低,可用稀释法使其析出,这种方法的优点是操作简便,费用低,副产物废硫酸母液便于回收和利用。)稀释盐析法(许多芳磺酸盐在水中的溶解度很大,但是在相同正离子的存在下,则溶解度明显下降,因此可以向磺化稀释液中加入氯化钠、硫酸钠、或钾盐等,使芳磺酸盐析出来);中和盐析法 (可用碳酸钠、氢氧化钠、氨水等中和盐析);脱硫酸钙法;溶剂萃取法。
反应方程式如下:
![]()
![]()
三、产品性质:
白色浆状物或粉末。具有去污、湿润、发泡、乳化、分散等性能。生物降解度>90%。在较宽的 pH 范围内比较稳定。其钠或铵盐呈中性,能溶于水,对水硬度不敏感,对酸、碱水解的稳定性好。它的钙盐或镁盐在水中的溶解度要低一些,但可溶于烃类溶剂中,在这方面也有一定的应用价值。
四、仪器和药品:
仪器:搅拌器、温度计(0℃~100℃)、滴液漏斗(60ml)、回流冷凝器、250mL四口瓶、分液漏斗(60ml)。
药品:十二烷基苯、98%硫酸、10%氢氧化钠溶液、氯化钠。
五、实验步骤:
1、磺化:
在装有搅拌器、温度计、滴液漏斗和回流冷凝器的250mL四口瓶中,加入十二烷基苯35mL(34.6g),搅拌下缓慢加入质量分数98%硫酸35mL,温度不超过40℃,加完后升温至60~70℃,反应2h。
2、分酸:
将上述磺化混合液降温至40~50℃,缓慢滴加适量水(约15mL),倒入分液漏斗中,静止片刻,分层,放掉下层(水和无机盐),保留上层(有机相)。
3、中和:
配制质量分数10%氢氧化钠溶液80mL,将其加入250mL四口瓶中约60~70mL,搅拌下缓慢滴加上述有机相,控制温度为40~50℃,用质量分数10%氢氧化钠调节pH=7~8,并记录质量分数10%氢氧化钠总用量。
4、盐析:
于上述反应体系中,加入少量氯化钠,渗圈试验清晰后过滤,得到白色膏状产品。
六、注意事项
1、分酸时,温度不可过低,否则易使分液漏斗被无机盐堵塞,造成分酸困难。
产率计算
十二烷基苯35mL(34.6g),98%硫酸35mL,适量水(约15mL),10%氢氧化钠溶液80mL
![]()
246.43 326.49
0.14
![]()
326.49 348.48
n =m/M=34.6g/246.43=0.14mol
理论产量:m=n*M=0.14*348.48=48.7873g(十二烷基苯磺酸钠)
我们欢迎各方(自)媒体、机构转载、引用我们原创内容,但需严格注明来源。同时,我们也倡导尊重与保护知识产权,如发现文章内容涉及侵权,请通过在线咨询进行投诉,我们会在第一时间核实处理。














 分子式:C18H29NaO3S
分子式:C18H29NaO3S


